Antiepileptika bei neuropathischen Schmerzen
- Autor(en): Urspeter Masche
- Reviewer: Michele Curatolo, Walter Friedli, Mathias Sturzenegger, Martin Tramèr
- pharma-kritik-Jahrgang 27
, Nummer 15, PK137
Redaktionsschluss: 27. Mai 2006
DOI: https://doi.org/10.37667/pk.2005.137 - PDF-Download der Printversion dieser pharma-kritik Nummer
Als neuropathisch werden Schmerzen bezeichnet, die sich als Folge einer Krankheit, Läsion oder Dysfunktion des peripheren oder zentralen Nervensystems entwickeln. Im Gegensatz zu nozizeptiven Schmerzen, die durch Stimulation von Schmerzrezeptoren entstehen, beruhen neuropathische Schmerzen auf einer abnormen Nervenleitung. Die Pathophysiologie neuropathischer Schmerzen ist noch wenig geklärt. Sie entstehen, wenn Funktion oder Struktur von schmerzvermittelnden Afferenzen gestört ist, wobei sowohl sensible Nerven in der Peripherie als auch afferente Rückenmarksbahnen oder zentrale Projektionsfelder betroffen sein können. Vermutlich führen Reparatur- und Reorganisationsvorgänge in den Nervenzellen dazu, dass die Balance der Neurotransmitter-Wirkungen gestört wird; auch lässt sich in den lädierten Axonmembranen eine Zunahme von Natriumkanälen beobachten, welche die ektope Reizbildung fördern. Infolge der vermehrten und veränderten afferenten Impulse reagiert das zentrale Nervensystem auf verschiedenen Ebenen (spinal, thalamisch) mit sekundären Veränderungen, was ebenfalls zu einer Übererregbarkeit beiträgt, gekennzeichnet durch eine erniedrigte Reizschwelle oder verstärkte Reizantwort.(1)
Beispiele von neuropathischen Schmerzsyndromen sind die Trigeminusneuralgie, die diabetische Neuropathie und die postherpetische Neuralgie. Sie stellen gut definierte Krankheitsbilder dar, weshalb bei ihnen praktisch alle wichtigen Studien durchgeführt wurden, die sich mit der medikamentösen Behandlung neuropathischer Schmerzen befassten. Eine weitere häufige Ursache neuropathischer Schmerzen bilden Nervenkompressionssyndrome (radikuläre Läsionen, periphere «Entrapment »-Syndrome). Die wichtigsten Krankheiten oder Zustände, bei denen neuropathische Schmerzen vorkommen können, sind in Tabelle 1 zusammengestellt; die Unterscheidung zwischen den häufigeren peripher vermittelten und den selteneren vom Zentralnervensystem ausgehenden Formen ist nur mit Vorbehalt möglich, da in den meisten Fällen sowohl periphere als auch zentrale Mechanismen von Bedeutung sind.(2)
Neuropathische Schmerzen äussern sich typischerweise als brennende oder schneidende Dauerschmerzen oder als elektrisierend einschiessende Schmerzattacken. Sie treten entweder spontan auf oder ausgelöst durch mechanische, thermische, chemische oder gar emotionale Trigger. Bei den reizinduzierten unterscheidet man zwischen der Allodynie (Schmerzen bei einem Reiz, der üblicherweise keine Schmerzen erzeugt) und der Hyperalgesie (verstärkte Schmerzen bei einem Reiz, der auch normalerweise Schmerzen verursacht). Jegliche Charakteristika neuropathischer Schmerzen manifestieren sich aber meistens nicht isoliert, sondern in gemischter Form. Als ein wesentliches Merkmal neuropathischer Schmerzen gilt, dass in der betroffenen Körperregion auch Parästhesien, Dysästhesien oder andere Sensibilitätsstörungen vorkommen.
Zur Quantifizierung neuropathischer Schmerzen dient zum Beispiel die weit verbreitete 11-stufige numerische Skala, bei der 0 keine Schmerzen und 10 die schlimmsten vorstellbaren Schmerzen bedeuten. Erfahrungsgemäss entspricht ein Wert bis ungefähr 4 einer Schmerzintensität, die für viele Leute erträglich ist, so dass sich erst oberhalb dieser Grenze eine Behandlungsindikation ergibt. Auf einer numerischen Skala sollte eine Schmerzlinderung mindestens 30% betragen, damit sie als klinisch relevant gewertet werden kann.(3) Für die detailliertere Beurteilung von neuropathischen Schmerzen existieren Skalen, in denen der Schmerz nicht nur quantitativ, sondern auch qualitativ erfasst wird. (z.B. «McGill Pain Questionnaire»).
Die Behandlung von neuropathischen Schmerzen ist mehrheitlich symptomatisch, da sich die Grundlage bzw. der ursächliche Faktor selten entscheidend beeinflussen lässt. Ausnahmen, bei denen kausale Therapien im Vordergrund stehen, bilden Neuropathien, die mit Infektionen zusammenhängen (Borreliose, Herpes zoster) oder die durch einen Mangelzustand bedingt sind (z.B. Vitamin-B12-Mangel) sowie das Guillain- Barré-Syndrom; ferner scheint es bei der diabetischen Neuropathie, dass eine gute Blutzuckereinstellung zur Schmerzlinderung beiträgt. Bei der symptomatischen Behandlung stellen systemisch verabreichte Medikamente diejenige Option dar, die am besten untersucht ist. Allerdings kann man bestenfalls eine Abnahme der Schmerzen um 30 bis 50% erwarten. Deshalb ist auch an andere Massnahmen zu denken, die sich im Einzelfall als durchaus nützlich erweisen können. Es handelt sich einerseits um Medikamente, die lokal appliziert werden, wie Lidocain als Pflaster (Neurodol® Tissugel) oder Capsaicin als Crème, andererseits um invasive Schmerzinterventionen, physikalische Massnahmen (z.B. transkutane elektrische Nervenstimulation = TENS) oder psychologische Verfahren (Entspannungsübungen, kognitive Verhaltenstherapie).
Unter den Medikamenten versprechen diejenigen die beste Wirkung, welche über die Beeinflussung von Neurotransmittern oder über andere Mechanismen die Schmerzübertragung beeinflussen. Als Mittel der ersten Wahl gelten trizyklische Antidepressiva und Antiepileptika. Möglicherweise ähnlich wirksam sind Opioide, wobei dazu aber deutlich weniger Daten existieren als zu den Antidepressiva oder Antiepileptika. Praktisch keinen Effekt haben peripher wirkende Analgetika wie nicht-steroidale Entzündungshemmer.
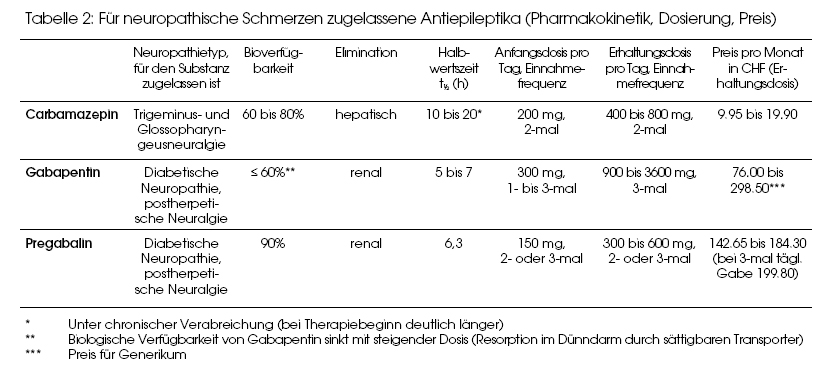
Trizyklische Antidepressiva wie Amitriptylin (Saroten® Retard, Tryptizol®) waren die erste Medikamentengruppe, zu denen aussagekräftige Studien zur Wirkung bei neuropathischen Schmerzen vorlagen. Wenn man eine Schmerzabnahme um mindestens 50% als Mass nimmt, liegt die «number needed to treat» (NNT) bei trizyklischen Antidepressiva zwischen 2 und 3.(4) Selektive Serotonin-Wiederaufnahmehemmer (SSRI) und andere neuere Antidepressiva haben sich als weniger wirksam erwiesen bzw. sind weniger untersucht als trizyklische Substanzen. Auch Antiepileptika haben in der Schmerzbehandlung eine lange Tradition; man denkt dabei vor allem an Carbamazepin (Tegretol® u.a.) zur Behandlung der Trigeminusneuralgie. Auf welche Weise Antiepileptika neuropathische Schmerzen zu beeinflussen vermögen, ist nicht exakt geklärt. Neuere Antiepileptika werden heute gegenüber trizyklischen Antidepressiva oft bevorzugt (die im Ruf stehen, schlechter verträglich zu sein). In den folgenden Abschnitten wird deshalb detaillierter auf einzelne Antiepileptika eingegangen. Tabelle 2 liefert zusätzliche Angaben zu den drei Antiepileptika, die in der Schweiz für einzelne Formen neuropathischer Schmerzen zugelassen sind.Ältere Antiepileptika
Phenytoin
Phenytoin (Phenhydan® u.a.) wurde als erstes Antiepileptikum zur Schmerzbehandlung eingesetzt. Basierend auf der Beobachtung, dass die Schmerzattacken der Trigeminusneuralgie einem epileptischen Anfall ähneln, wurde es vor über 60 Jahren mit Erfolg bei diesem Leiden versucht. In kontrollierten Studien wurde Phenytoin nur bei anderen Formen neuropathischer Schmerzen geprüft, wobei sich kein eindeutiger Effekt zeigte. Bei der diabetischen Neuropathie ergaben zwei Studien gar gegensätzliche Resultate. Daraus muss gefolgert werden, dass Phenytoin zur Behandlung neuropathischer Schmerzen nicht geeignet ist.(5,6)
Carbamazepin
Auch Carbamazepin wurde bald nach seiner Einführung bei der Trigeminusneuralgie verwendet und gilt für diese Indikation (sowie für die verwandte Glossopharyngeusneuralgie) immer noch als Mittel der ersten Wahl. Gemäss einer Cochrane- Zusammenstellung gibt es sieben kontrollierte Studien, in denen Carbamazepin bei Trigeminusneuralgie untersucht wurde, wobei die Wirkung des Medikamentes viermal mit derjenigen von Placebo und dreimal mit derjenigen anderer Substanzen verglichen wurde. Dabei erwies sich Carbamazepin signifikant wirksamer als Placebo und Tizanidin (Sirdalud®), gleich wirksam wie das Antiarrhythmikum Tocainid (Xylotan®, nicht mehr im Handel) und weniger wirksam als das Neuroleptikum Pimozid (Orap®, in der Schweiz nicht mehr im Handel).(7)
Mit Carbamazepin sind auch bei anderen Neuropathieformen ein paar kleine Studien durchgeführt worden. Die Cochrane- Arbeit liefert dazu ebenfalls eine Übersicht: Bei der diabetischen Neuropathie war Carbamazepin signifikant wirksamer als Placebo und zeigte eine vergleichbare Wirkung wie die Kombination von Nortriptylin (Nortrilen®) mit Fluphenazin (Dapotum®). Bei postherpetischer Neuralgie erwies sich Carbamazepin in Kombination mit Clomipramin (Anafranil®) gegenüber einer TENS-Behandlung als überlegen. Bei neuropathischen Schmerzen nach Schlaganfall nützten weder Carbamazepin noch Amitriptylin mehr als Placebo.
Eine Behandlung mit Carbamazepin muss besonders zu Beginn sorgfältig überwacht werden, zum einen weil es wegen der Induktion des eigenen Metabolismus eine genaue Dosierung erfordert, zum anderen weil es vielfältige Nebenwirkungen verursachen kann (neurologische und psychiatrische Nebenwirkungen, Hyponatriämien, Zytopenien, Überempfindlichkeitsreaktionen mit Beteiligung von Haut, Leber oder anderen Organen).
Andere ältere Antiepileptika
Für Valproinsäure (Convulex® u.a.) wird anhand von Fallserien ein günstiger Effekt bei Trigeminusneuralgie und anderen neuropathischen Schmerzzuständen beschrieben. Aus den wenigen kontrollierten Studien, die durchgeführt wurden, lässt sich jedoch kein überzeugender Nutzen ableiten.(5,8,9)
Clonazepam (Rivotril®) und andere Benzodiazepine wurden
ebenfalls bei neuropathischen Schmerzen versucht, wobei sich aber eine positive Wirkung durch kontrollierte Studien bislang nicht belegen liess.(5)
Neuere Antiepileptika
Gabapentin
Gabapentin (Neurontin® u.a.) hat eine ähnliche chemische Struktur wie die gamma-Aminobuttersäure (GABA). Die Wirkung lässt sich indessen weder auf eine Bindung an GABA-Rezeptoren noch auf eine Veränderung des GABA-Metabolismus zurückführen, sondern beruht auf anderen Mechanismen.
Wie aus einer Metaanalyse hervorgeht, wirkt Gabapentin bei diabetischer Neuropathie und postherpetischer Neuralgie signifikant besser als Placebo; als NNT errechnete sich ein Wert von etwa 3 bis 4 (unter Annahme einer mindestens mittelgradigen Schmerzlinderung als Endpunkt).(10) Orientiert man sich mehr am praktischen Alltag, scheint der Unterschied gegenüber Placebo aber geringer zu sein. So kam man in einer Studie, die verschiedene Neuropathieformen umfasste (als Einschlusskriterium zahlte das Symptom "neuropathischer Schmerz" und nicht ein bestimmtes Syndrom), auf eine höhere NNT von 13.(11) In zwei kleinen Studien wurde Gabapentin bei diabetischer Neuropathie auch mit Amitriptylin verglichen, wobei sich keine signifikanten Unterschiede ergaben.(10)
Etwa 20 bis 25% der Gabapentin-Behandelten klagen über Schwindel und Schläfrigkeit. Andere Nebenwirkungen sind gastrointestinale Beschwerden, Kopfschmerzen, Ataxie, Tremor, Verwirrtheit, Sehstörungen und Ödeme. Um das Risiko von Nebenwirkungen zu reduzieren, sollte man die Therapie mit einer niedrigen Tagesdosis von 300 mg beginnen und sukzessive auf mindestens 900 mg steigern. Als maximale Tagesdosen wurden in den vorliegenden Studien 2400 bis 3600 mg verwendet.
Pregabalin
Das kurzlich eingefuhrte Pregabalin (Lyrica®) ist strukturell dem Gabapentin nahe verwandt, weshalb die beiden Substanzen die pharmakologischen Eigenschaften sowie die Indikationen teilen. Im Vergleich zu Gabapentin weist Pregabalin eine höhere und dosisunabhängige biologische Verfügbarkeit auf, ansonsten finden sich auch bei der Pharmakokinetik keine nennenswerten Unterschiede.
Die Wirkung von Pregabalin bei neuropathischen Schmerzen wurde in zwölf placebokontrollierten Doppelblindstudien bei Personen mit diabetischer Neuropathie oder postherpetischer Neuralgie untersucht. Abgesehen von der Dauer (5 bis 13 Wochen) kannten alle Studien einen ähnlichen Aufbau. Die Pregabalin-Tagesdosen bewegten sich zwischen 75 und 600 mg, verteilt auf zwei bis drei Dosen pro Tag; in den meisten Studien wurde das Medikament über die ersten 1 bis 2 Wochen auf die Zieldosis titriert. Als Begleitmedikamente waren auch Antidepressiva erlaubt, sofern deren Dosierung konstant gehalten wurde. Zu Beginn der Studien gaben die Teilnehmenden eine durchschnittliche Schmerzstärke zwischen 6 und 7 auf einer numerischen 11-Punkte-Skala an. In den Placebogruppen nahmen die Schmerzen um 0,3 bis 1,7 Punkte ab. Bei Pregabalin waren es mit einer Tagesdosis von 75 mg 1,2 bis 1,8, mit 150 mg 0,9 bis 1,9, mit 300 mg 1,6 bis 2,5 und mit 600 mg 2,4 bis 3,2 Punkte; eindeutig signifikante Unterschiede gegenüber Placebo ergaben sich nur mit den Pregabalin-Dosen von 300 und 600 mg/Tag. Die Ansprechrate, definiert als mindestens 50%ige Abnahme der Schmerzstärke, erreichte in den Placebogruppen 8 bis 30%, bei den Pregabalin-Behandelten 19 bis 52%. Die entsprechende NNT liegt zwischen 3 und 7 (d.h. 3 bis 7 Patienten mussen mit Pregabalin behandelt werden, damit sich bei 1 die Schmerzintensität halbiert).
Einige der Studien wurden über längere Zeit offen weitergeführt. Es zeigte sich dabei, dass die Wirkung aufrechterhalten blieb und man nicht mit einer Toleranzentwicklung rechnen muss.(12,13)
Typische Nebenwirkungen von Pregabalin sind wie bei Gabapentin Schwindel und Somnolenz, was – besonders bei älteren Leuten – mit einer erhöhten Sturzgefahr verbunden sein könnte. Auch sonst haben die beiden Substanzen ein ziemlich identisches Nebenwirkungsspektrum. Ferner sind unter Pregabalin Fälle von Gesichtsfeldausfällen vorgekommen; ein Kausalzusammenhang wird zwar als unwahrscheinlich betrachtet, kann aber nicht ausgeschlossen werden. Bei Mäusen entwickelten sich nach einer längeren Pregabalin-Exposition von über zwei Jahren Hämangiosarkome, die über eine Thrombozytenaktivierung zustandegekommen waren. Man nimmt an, dass dieses Risiko für den Menschen nicht zutrifft; für mehr Gewissheit wird es aber weitere Langzeitdaten brauchen.
Andere neuere Antiepileptika
Oxcarbazepin (Trileptal®) scheint bei Trigeminusneuralgie ebenso wirksam zu sein wie Carbamazepin.(14) Bei diabetischer Neuropathie ist Oxcarbazepin in einer Studie geprüft worden, wobei es die Schmerzen signifikant mehr reduzierte als Placebo.(15)
Auch Lamotrigin (Lamictal®) und Topiramat (Topamax®) sind bei neuropathischen Schmerzen eingesetzt worden. Allerdings liessen sich die positiven Resultate, die sich in Fallserien und offenen Studien ergaben, unter kontrollierten Bedingungen bis anhin nicht eindeutig reproduzieren.(5,9)
Schlussfolgerungen
Bevor man sich bei neuropathischen Schmerzen zu einer symptomatischen Therapie entschliesst, sollten immer zuerst diejenigen Ursachen ausgeschlossen werden, bei denen eine kausale Behandlung existiert. Gut untersucht ist die medikamentöse Behandlung von neuropathischen Schmerzen lediglich bei der Trigeminusneuralgie, der diabetischen Neuropathie und der postherpetischen Neuralgie. Für die Trigeminusneuralgie ist Carbamazepin die Standardsubstanz. Bei den anderen Formen wird dieser Platz unter den Antiepileptika von Gabapentin eingenommen. Pregabalin, das als Neuentwicklung propagiert wird, verspricht gegenüber Gabapentin keinen relevanten Vorteil. Die Einführung von Pregabalin ist vor allem als Antwort darauf zu verstehen, dass von Gabapentin unterdessen Generika auf den Markt drängen.(16)
Ob Gabapentin zu Recht bei neuropathischen Schmerzen das am meisten verschriebene Mittel ist, lässt sich in Frage stellen. Trizyklische Antidepressiva kann man sicher als gleich wirksam einstufen. Auch bei der Verträglichkeit findet man keine klaren Unterschiede: gemäss einer aktuellen Metaanalyse beträgt die «number needed to harm» (NNH) für die trizyklischen Antidepressiva 15, für Gabapentin 26 und für Pregabalin 12, wobei die Differenzen nicht signifikant sind (die NNH gibt an, wieviele Leute behandelt werden können, bis jemand wegen einer Nebenwirkung die Studie oder die Therapie abbrechen muss).(4) Inwieweit sich das Bild bei älteren Leuten änderte, die auf trizyklische Antidepressiva, womöglich aber eben auch auf Antiepileptika empfindlicher reagieren, bleibt offen. Von Bedeutung sind solche Überlegungen auch, weil eine Behandlung mit trizyklischen Antidepressiva erheblich billiger ist als mit Gabapentin oder Pregabalin.
Sowohl mit Antiepileptika wie mit anderen Medikamenten kann man höchstens in Ausnahmefällen eine vollständige Linderung von neuropathischen Schmerzen erreichen. Es scheint, dass sich das Ansprechen zuweilen verbessern lässt, wenn man Substanzen aus verschiedenen Gruppen zusammen verabreicht (z.B. Kombination von Antiepileptika oder trizyklischen Antidepressiva mit Opioiden).
Literatur
- 1) Nicholson B. Acta Neurol Scand 2000; 101: 359-71
- 2) Dworkin RH et al. Arch Neurol 2003; 60: 1525-34
- 3) http://www.hc-sc.gc.ca/dhp-mps/prodpharma/activit/sci-consult/neuropath/ sapnp_rop_gcsdn_crd_2004-12-02_e.html
- 4) Finnerup NB et al. Pain 2005; 118: 289-305
- 5) Tremont-Lukats IW et al. Drugs 2000; 60: 1029-52
- 6) Wiffen P et al. Cochrane Database Syst Rev 2005 Jul 20; 3: CD001133
- 7) Wiffen PJ et al. Cochrane Database Syst Rev 2005 Jul 20; 3: CD005451
- 8) Spina E, Perugi G. Epileptic Diosord 2004; 6: 57-75
- 9) Vinik A. J Clin Endocrinol Metab 2005; 90: 4936-45
- 10) Wiffen PJ et al. Cochrane Database Syst Rev 2005 Jul 20; 3: CD005452
- 11) Serpell MG. Pain 2002; 99: 557-66
- 12) http://www.emea.eu.int/humandocs/PDFs/EPAR/lyrica/084504en6.pdf
- 13) Hadj Tahar A. Issues Emerg Health Technol 2005; (67): 1-4
- 14) Guay DR. Am J Geriatr Pharmacother 2003; 1: 18-37
- 15) Dogra S et al. Eur J Pain 2005; 9: 543-54
- 16) http://www.bioportfolio.com/news/datamonitor_38.htm
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK137
Verwandte Artikel
LoginGratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.